Консорциум по генетике РРССВ-хозяина (PRRS Host Genetics Consortium=PHGC) был, при участии Джоан Ланни (ARS USDA) и Джека Деккерса (Университет штата Айова), создан как средство, позволяющее внедрить использование геномных и генетических инструментов для уменьшения неблагоприятного воздействия РРСС. В своей работе он комбинирует шедевральные вирусологические-иммунологические методики с генетическими-геномными. Основную практическую выгоду дает использование результатов в коммерческих программах по выращиванию животных. В предпринимавшихся до сей поры попытках идентифицировать гены, отвечающие за сопротивляемость болезни, исследователи фокусировались на сравнении реакции на болезнь у свиней различных чистопородных линий. PHGC не сравнивает породы, а занят исключительно идентифицированием маркеров сопротивляемости/подверженности инфекции, присутствующих в промышленно-выращиваемых поголовьях животных, демонстрирующих целый спектр различных фенотипов болезни. Модель PHGC заключается в экспериментальном заражении двухсот молодых свиней хорошо изученными вирусами РРСС. Среди важнейших фенотипических данных, фиксируемых по каждому такому животному: смертность, вирусная нагрузка в сыворотке крови, набор массы, уровни нейтрализующих антител и цитокина (примеры см. на Рис.1). Генотипирование всех свиней свиным чипом 60К SNP и проведение исследований по широкому геномному ассоциированию позволило выявить несколько маркеров, связанных с развитием манифестации болезни и сопротивляемости ей. «Благоприятный» аллель одного из важных маркеров на 4 хромосоме Sus scrofa (SSC4) был ассоциирован с ростом набора массы и снижением вирусной нагрузки. За 42 дня периода экспериментального инфекционного заражения, свиньи с благоприятствующим генотипом набрали почти на 10% больше массы и продемонстрировали соответсвующее снижение виремии. Результат влияния благоприятного генотипа представлен на Рис.2. Последние данные свидетельствуют о том, что подобных выгод от «благоприятного» аллеля можно добиться в условиях реального производства.

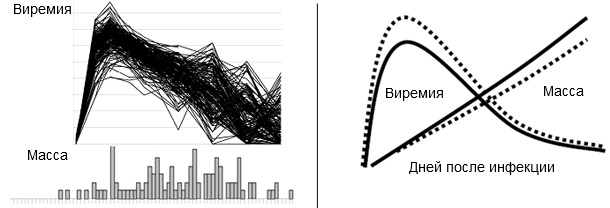
| Рис.1. Фенотипы болезни, вызываемой вирусом РРСС, на уровне поголовья. Вышеприведенные цифры показывают виремию РРССВ (верхн.) и распределение набора массы (нижн.) у 200 свиней, экспериментально зараженных вирусом РРСС. Инфицирование состоялось по достижении поросятами возраста 3 недели, данные фиксировались на протяжении 42-х дней после инфицирования. | Рис.2. Благотворное влияние маркера в SSC4 на набор массы и веремию у поросят. Вышеприведенная модель показывает ожидаемые улучшения в привесах и виремии у свиней с «благоприятным» аллелем (АВ или ВВ, сплошная линия), по сравнению с поросятами с генотипом АА (прерывистая линия). Рост привесов достигает около 10%. Снижение пика виремии – приблизительно 1 log. |
Дополнительные фенотипические результаты связаны с различными аспектами РРССВ-специфичного иммунитета. Например, нами была выявлена обратная связь между вирусной нагрузкой и нейтрализующим вирус титром. Кроме того, у небольшого процента инфицированных свиней развивается уникальный гуморальный иммунный ответ, который можно описать как широко нейтрализующий – обладающий способностью нейтрализовывать широкий спектр изолятов, включя вирусы I-типа. И хотя в таком нейтрализующем ответе наследственный компонент не выявлен, он присутствует в уровне анти-N протеин-специфичных антител и связан с SNP на SSC7. Маркер на SSC1 коррелирует с тяжким респираторным заболеванием у свиней с КРБС. Ближайший геномный маркер находится вблизи с воспалительным цитокиновым рецептором.
Результаты проведенной PHGC работы содержат важные открытия. Во-первых, в манифестации болезни и последствиях, вызываемых РРСС-инфекцией, присутствуют важные наследственные компоненты. Во-вторых, относительно небольшое число геномных маркеров ассоциируется с данным фенотипом болезни. Это делает возможным использование проводимого по маркерам отбора для выведения свиней с повышенной сопротивляемостью инфекции. И, наконец, по последним данным, все геномные маркеры, связанные с клиническими проявлениями (манифестацией) болезни и иммунитетом, расположены на таких участках генома свиньи, на которых содержатся иммунологически-релевантные гены, включая интерферон-стимулированные гены, гены MHC и цитокинового ответа. В заключение, геномика и генетика являются новыми инструментами, помогающими защитить здоровье животных. Особенно это важно в тех случаях, когда речь идет об инфекционных заболеваниях, против которых нет действенных вакцин или лекарств. Если улучшенную генетику использовать совместно с улучшенными вакцинами и все это будет происходить в условиях улучшенного питания, то множество негативных факторов эндемичной РРСС могут быть преодолены.


